איך קוראים לתרכובות כימיות
מְחַבֵּר:
Laura McKinney
תאריך הבריאה:
2 אַפּרִיל 2021
תאריך עדכון:
26 יוני 2024

תוֹכֶן
- בשלבים
- שיטה 1 שמות של תרכובות יוניות
- שיטה 2 שמות של תרכובות פוליאטומיות
- שיטה 3 שמות של תרכובות קוולנטיות
להצליח בתחום הכימיה דורש לדעת איך לקרוא לתרכובות הכימיות הבסיסיות. מדריך זה מספק לך כללים בסיסיים על תהליך השמות לתרכובות כימיות וכיצד להקצות שמות לתרכובות שאינן מוכרות לך.
בשלבים
שיטה 1 שמות של תרכובות יוניות
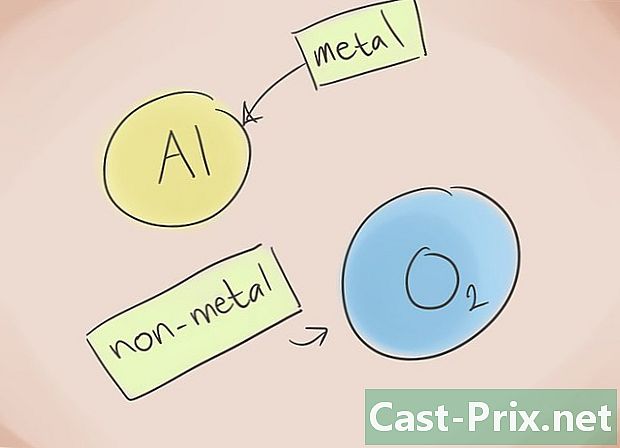
- מהו תרכובת יונית? תרכובות יוניות מורכבות ממתכת ולא מתכת. לאחר מכן עיין בטבלת האלמנטים התקופתיים כדי לדעת אילו קטגוריות שייכות ליסודות הקיימים במתחם.
-

טופס את השם. אין דבר קל יותר מאשר שמות של תרכובת יונית של שני אלמנטים. אכן, החלק הראשון של שם המתחם תואם את שמו של האלמנט הלא-מתכתי הנושא את הסיומת "ure" ואילו השני תואם את שם האלמנט המתכתי. ישנם יוצאים מן הכלל: תחמוצת, פוספיד, ניטריד, סולפיד.- דוגמה: Al2O3. אל2 = אלומיניום; O3 = חמצן. אז שם המתחם יהיה "תחמוצת אלומיניום".
-
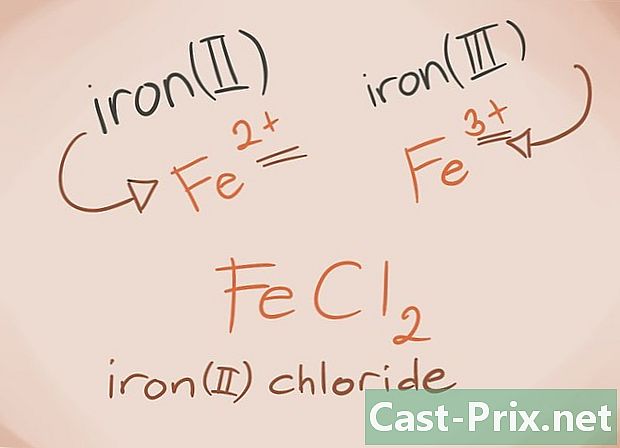
הכירו את מתכות המעבר מתכות המעבר הן אלה שנמצאות בלוקי D ו- F של הטבלה המחזורית. בשם המתחם, המטען על מתכות אלה כתוב בספרות רומיות. הסיבה לכך היא שמתכות מעבר יכולות לשאת עומס רב יותר וליצור יותר תרכובת.- דוגמה: FeCl2 ו- FeCl3. Fe = ברזל; Cl2 = -2 כלוריד; Cl3 = כלוריד -3. כשמות, יהיו כלוריד ברזלי (II) וכלוריד ברזלי (III).
שיטה 2 שמות של תרכובות פוליאטומיות
-

עליכם להבין מהו תרכובת פוליאטומית. תרכובות פוליאטומיות הן תרכובות הנוצרות על ידי קבוצת דאטומים הקשורה זו בזו; כל הקבוצה הנושאת חיוב היא חיובית או שלילית. לאחר מכן ישנן שלוש פעולות בסיסיות שתוכלו לבצע על תרכובות פוליאטומיות:- אתה יכול להוסיף מימן לחלק הראשון של המתחם. המילה "מימן" אכן מתווספת בתחילת שם המתחם. זה יקטין את ערך המטען השלילי בזה אחר זה. לדוגמה, CO "פחמתי"3 הופך ל- HCO "מימן קרבונט"3.

- אתה יכול גם להסיר חמצן מהתרכובת. העומס לא משתנה, אך הסיומת "-איטית" של המתחם משתנה ל"אישיות ". למשל הטרנספורמציה של: NO3 ב- NO2 אנו עוברים מחנקה לחנקה. "

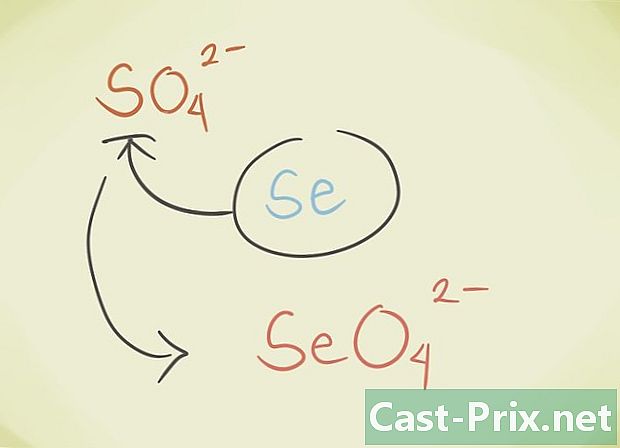
- ניתן להחליף את הלוטום המרכזי של המתחם באטום אחר השייך לאותה קבוצה תקופתית. לדוגמא, SO סולפט4 ניתן להחליף על ידי Selenate SeO4.
- אתה יכול להוסיף מימן לחלק הראשון של המתחם. המילה "מימן" אכן מתווספת בתחילת שם המתחם. זה יקטין את ערך המטען השלילי בזה אחר זה. לדוגמה, CO "פחמתי"3 הופך ל- HCO "מימן קרבונט"3.
-

שינן את קבוצות הדיון הנפוצות ביותר. הקבוצות שלהלן משמשות ליצירת רוב התרכובות הפוליומטיות. בעקבות הסדר ההולך וגובר של המטען השלילי שלהם, יש לנו:- יוני הידרוקסיד: OH
- יוני חנקה: NO3
- יוני מימן קרבונט: HCO3
- יוני פרמנגנט: MnO4
- יוני קרבונט: CO3
- יוני כרומט: CrO4
- יוני דיכרומט: Cr2O7
- יוני סולפט: SO4
- יוני סולפיט: SO3
- יוני תיוסולפט: S2O3
- יוני פוספט: PO4
- יוני אמוניום: NH4
- צרו שמות מורכבים מהרשימה שלמעלה. צרו קשר עם כל אחד מהפריטים שקשורים לקבוצה. אם האלמנט ממוקם לפני הקבוצה היונית, פשוט שם האלמנט יתווסף לתחילת שם המתחם.
- דוגמה: KMnO4. אתה בטח יכול לדעת את האריה MNO4 מתאים לפרמנגנט האריות. K מתייחס לאשלגן. אז המתחם שלך ייקרא פרמנגנט אשלגן.
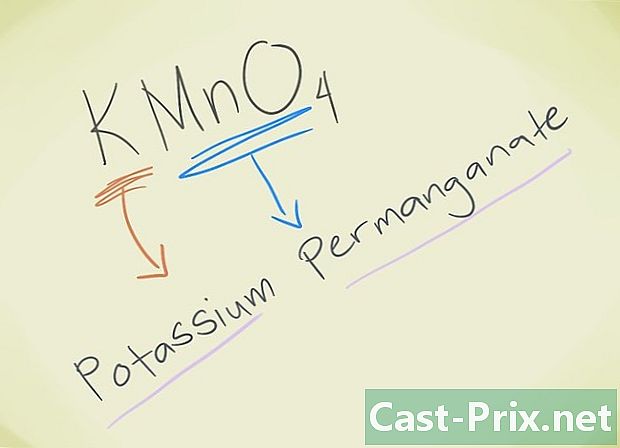
- דוגמה: NaOH. כנראה שתבינו כאן שזה OHOH. Na הוא נתרן, ולכן התרכובת תיקרא נתרן הידרוקסיד.

- דוגמה: KMnO4. אתה בטח יכול לדעת את האריה MNO4 מתאים לפרמנגנט האריות. K מתייחס לאשלגן. אז המתחם שלך ייקרא פרמנגנט אשלגן.
שיטה 3 שמות של תרכובות קוולנטיות
-
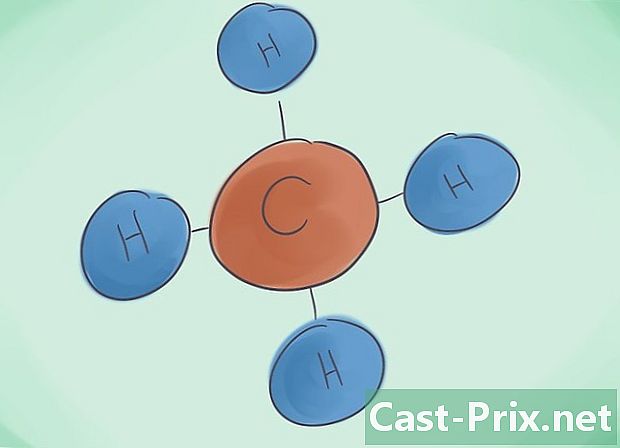
מהו תרכובת קוולנטית? התרכובות הקוואלנטיות נובעות מהקשר של לפחות שני יסודות לא מתכתיים. שם המתחם נקבע על פי מספר התאומים המהווים אותו. הקידומת היוונית שליד שם זה מציינת את מספר המולקולות הקיימות בתרכובת. -
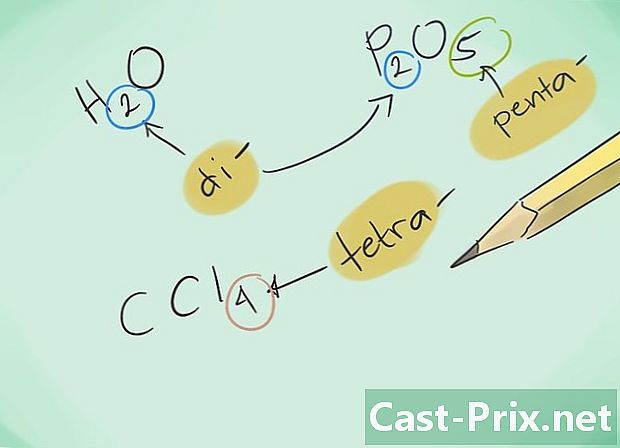
הכיר את הקידומות. שינן את הקידומות הבאות לתרכובות של 1 עד 8 אטומים:- אטום 1 - "מונו-"
- 2 אטומים - "די-"
- 3 אטומים - "Tri-"
- 4 אטומים - "טטרה-"
- 5 אטומים - "פנטה-"
- 6 אטומים - "Hexa-"
- 7 אטומים - "הפטה-"
- 8 אטומים - "אוקטה-"
- ואז תן שם לתרכובות. תן שם לתרכובת שנוצרה באמצעות הקידומות המתאימות. הקידומות צריכות להיות מושתלות על כל אחד מהיסודות המהווים תרכובת עם מספר אטומים.
- דוגמה: CO יחזור לפחמן חד חמצני בזמן CO2 ייעד פחמן דו חמצני.
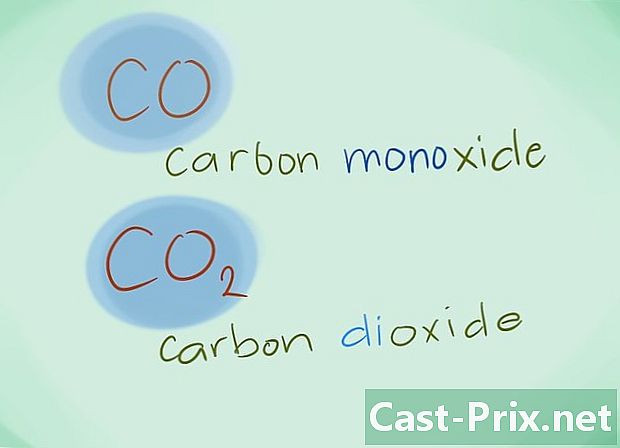
- דוגמא: נ2S3 יתכתב עם טריוסולפיד חנקתי.

- ברוב המקרים ניתן להשמיט את הקידומת "מונו"; זה, יותר מכל חוסר קידומת, גורם לכך שיש להשתמש באחרון. הקידומת הזו ממשיכה לשמש במקרה של פחמן חד חמצני בהתחשב בעובדה שהשימוש הזה חוזר לגליזים הראשונים של הכימיה.
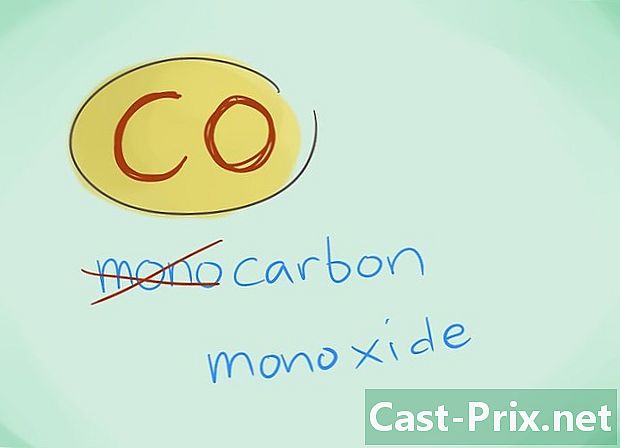
- דוגמה: CO יחזור לפחמן חד חמצני בזמן CO2 ייעד פחמן דו חמצני.
- כמובן שאתה חושד שמספר חריגים חלים על כל הכללים הללו; החזק לדוגמה את הנוסחה הזו, CaCl2אתה מצפה לראות את הכינוי "סידן דיכלוריד", שהוא לא. המתחם שלך פשוט ישמור את השם סידן כלוריד.
- יצוין גם כי כל זה אינו חל על כימיה אורגנית.
- הכללים המפורטים כאן מיועדים לקהל מתחיל בכימיה ומדע. ישנם כללים שונים מאוד כשאתם עוברים את שלב הכימיה המתקדם, כמו הכללים לגבי ערכי משתנה.